Ruxolitinib als neue Therapieoption bei atopischer Dermatitis
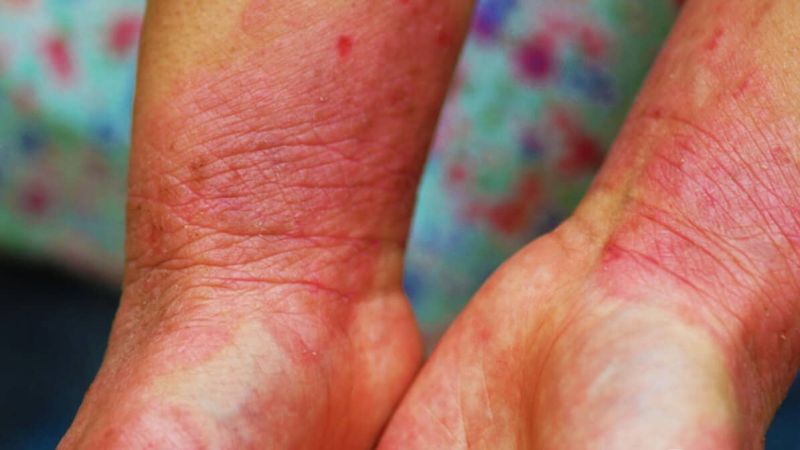
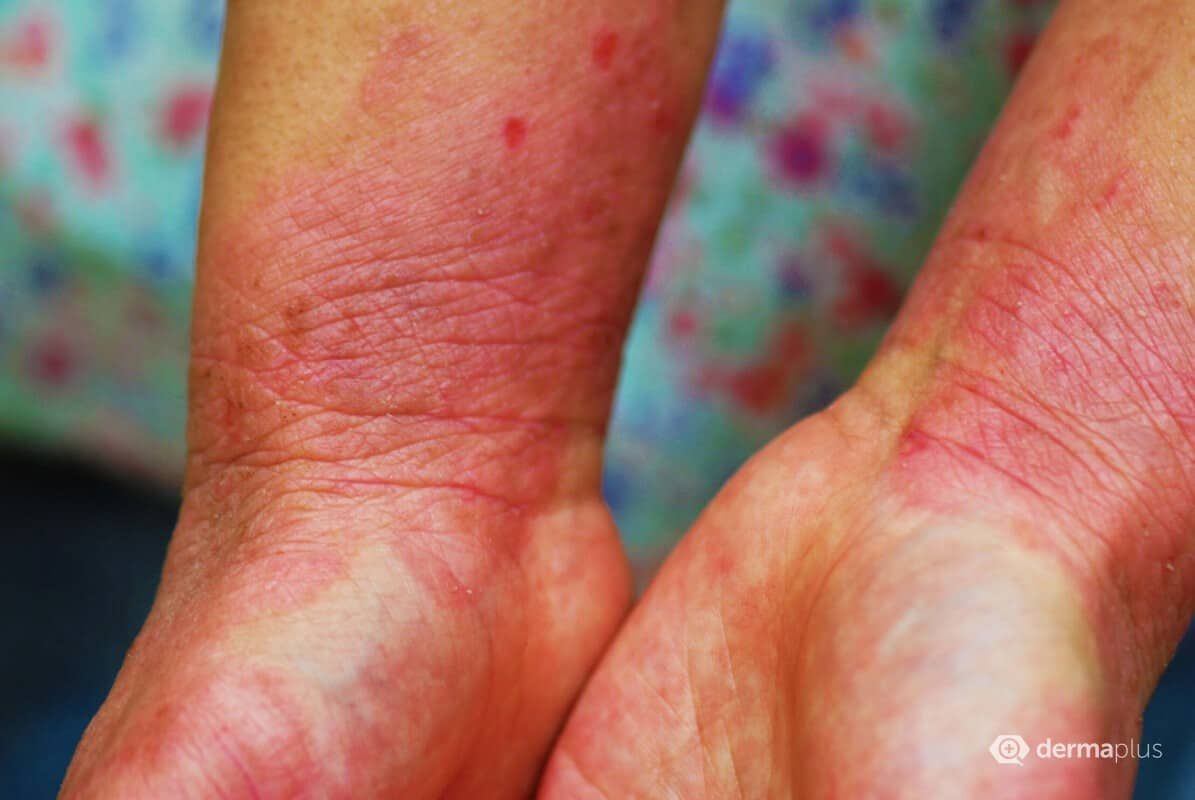
Die atopische Dermatitis (AD) ist eine chronische Entzündungskrankheit, die mit starkem Juckreiz einhergeht und die Lebensqualität der Betroffenen oft erheblich einschränkt. Sie tritt typischerweise bereits in den ersten Lebensjahren auf und ist bei Kindern mit einer Prävalenz von 10-20 % sehr häufig. Unter den Erwachsenen ist die Prävalenz mit je nach Region zwischen 5 und 10 % etwas niedriger. Zur topischen Behandlung werden vor allem entzündungshemmende Kortikosteroide und Calcineurininhibitoren eingesetzt. Insbesondere Kortikosteroide sind jedoch aufgrund ihres Nebenwirkungsprofils nicht für die langfristige Anwendung geeignet und dürfen darüber hinaus in bestimmten Regionen wie dem Gesicht nicht angewendet werden. Der Bedarf nach einer neuen, nicht-steroidalen topischen Therapieoption, die schnell und dauerhaft wirkt, ist deshalb groß.
Die Entzündungsantwort wird bei der AD im Wesentlichen durch Typ-2-Cytokine angetrieben und durch die Januskinasen JAK1 und JAK2 moduliert. Ein Hemmstoff dieser Enzyme könnte deshalb die Entzündung in einer frühen Phase unterdrücken. Allerdings haben auch JAK-Inhibitoren bei längerer Anwendung Nebenwirkungen; insbesondere können sie die Neubildung von Blutzellen im Knochenmark hemmen. Um dieses Risiko zu reduzieren, wurde zur Behandlung der AD eine topische Formulierung des JAK1/2-Hemmers Ruxolitinib entwickelt, die in einer klinischen Phase-2-Studie bereits ihre Wirksamkeit bei einem günstigen Nebenwirkungsprofil bewiesen hat. Nun haben zwei große klinische Phase-3-Studien an Erwachsenen und Jugendlichen dieses Ergebnis bestätigt.
Zwei Ruxolitinib-Dosierungen im Test
Die beiden Studien „Topical Ruxolitinib Evaluation in Atopic Dermatitis (TRuE-AD)“ hatten ein identisches Design (Tabelle 1): Sie waren randomisiert, doppelblind und Vehikel-kontrolliert. TRuE-AD1 wurde in 79, TRuE-AD2 in 66 Behandlungszentren in sieben nordamerikanischen und europäischen Ländern durchgeführt. Einschlusskriterien für die Studien waren ein Alter von mindestens 12 und eine Erkrankungsdauer von mindestens zwei Jahren, ein Investigator’s Global Assessment-(IGA)-Wert von 2/3 und eine betroffene Körperoberfläche (Body Surface Area, BSA) von 3-20 %. Die Patienten wurden 2:2:1 in drei Gruppen randomisiert: Gruppe 1 trug zweimal am Tag eine 0,75 %-Ruxolitinib-(RUX)-Creme auf die betroffenen Hautbereiche auf. Gruppe 2 verwendete zweimal am Tag 1,5 %-RUX, Gruppe 3 das wirkstofffreie Vehikel. Die Behandlung erfolgte bis zur Erhebung des primären Endpunkts an Tag 8, eine Rescue-Therapie war in dieser Zeit nicht erlaubt. Anschließend wurden die Probanden aus Gruppe 3 gleichmäßig auf die beiden Gruppen 1 und 2 aufgeteilt. Alle Studienteilnehmer erhielten dann für weitere 44 Wochen entweder 0,75 % oder 1,5 % RUX, um die Sicherheit der Langzeitanwendung zu bestimmen.
Tab. 1: Studiendesign TRuE-AD nach Papp et al. (2021)
| Erkrankung | atopische Dermatitis |
| Studienziel | Wirksamkeit und Sicherheit von Ruxolitinib |
| Studiendesign | randomisierte, doppelblinde, Vehikel-kontrollierte Interventionsstudie |
| Eingeschlossene Patienten | In TRuE-AD1: 631 In TRuE-AD2: 618 nach Ausschluss eines Studienorts gingen 577 in die primäre Endpunktanalyse ein |
| Intervention | Gruppe 1: 2x täglich 0,75 %-RUX für 8 Wochen (n = 252, n = 248) Gruppe 2: 2x täglich 1,5 % RUX für 8 Wochen (n = 253, n = 246) Gruppe 3: 2x täglich wirkstofffreies Vehikel für 8 Wochen (n = 126, n = 124) |
| Primärer Endpunkt | Anteil der Probanden mit Verbesserung des IGA |
| Sekundäre Endpunkte | u. a. Anteil der Patienten mit EASI-75, EASI-90, NRS4 |
| Sponsor | Incyte Corporation |
| Studienregisternummer | TRuE-AD1: NCT03745638, TRuE-AD2: NCT03745651 |
Untersuchung von Wirksamkeit und Sicherheit
In TRuE-AD1 wurden 631 Patienten zwischen 19 und 49 Jahren randomisiert, in TRuE-AD2 618 Patienten zwischen 20 und 52 Jahren (Tabelle 1). Der Anteil der Heranwachsenden lag in beiden Studien bei knapp 20 %. Für die Wirksamkeitsanalyse wurden alle randomisierten Patienten herangezogen, für die Sicherheitsanalyse nur jene, die mindestens eine Wirkstoffdosis erhalten hatten. Primärer Studienendpunkt war der Anteil der Patienten, die an Tag 8 eine Verbesserung des IGA um mindestens zwei Punkte im Vergleich zum Ausgangswert oder die einen Wert von IGA 0/1 erreicht hatten. Daneben wurden verschiedene sekundäre Endpunkte erhoben, die die Krankheitsschwere, den Leidensdruck sowie die Lebensqualität erfassten, darunter der Anteil der Patienten, die eine 75- bzw. 90 %ige Verbesserung auf dem Eczema Area and Severity Index (EASI-75, EASI-90) erreichten, die sich auf der Numerical Rating Scale zur Bestimmung des Juckreizes um mindestens vier Punkte verbesserten (NRS4) und die eine deutliche Verbesserung ihres Schlafs angaben. Zusätzlich wurden die unerwünschten Arzneimittelnebenwirkungen dokumentiert und die Wirkstoffkonzentration im Plasma gemessen.
Ruxolitinib verbessert das Hautbild und lindert Juckreiz
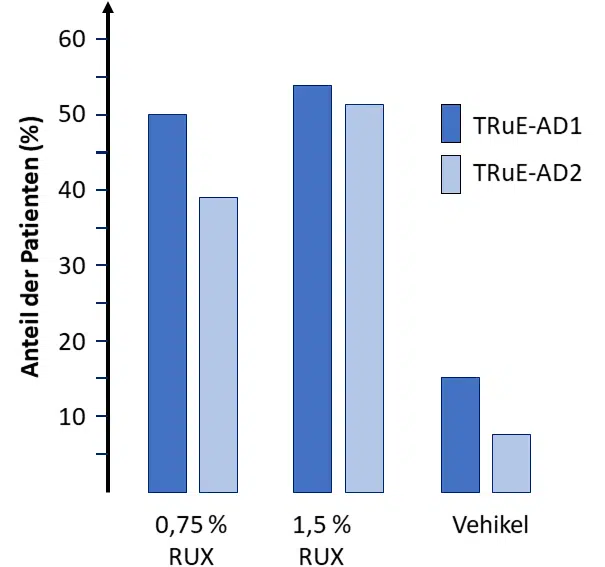
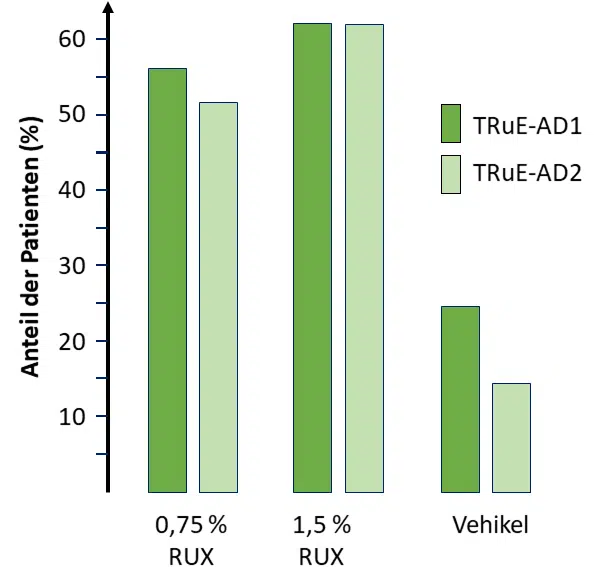
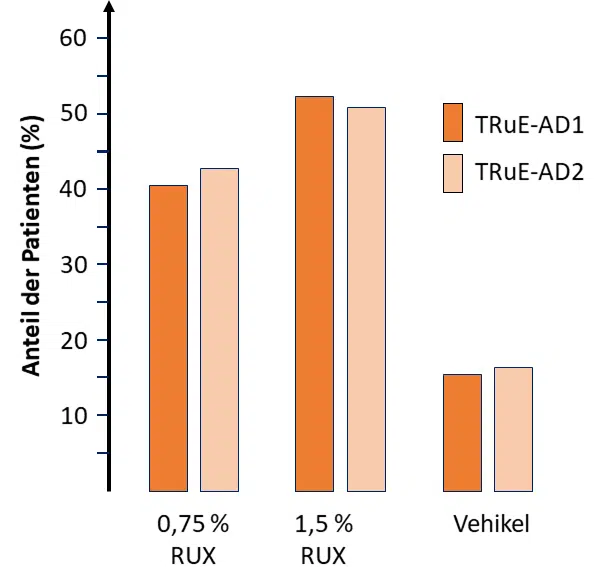
In beiden Studiengruppen erreichten signifikant mehr Patienten unter Ruxolitinib den primären Endpunkt (Abbildung 1). Dabei hatten beide Dosierungen einen ähnlich positiven Effekt. Ein vergleichbares Bild zeigte sich bei den EASI-Werten und dem NRS4: Sowohl EASI-75 und EASI-90 (Abbildung 2) als auch der NRS4 (Abbildung 3) wurden in den Wirkstoffgruppen von deutlich mehr Patienten erreicht als in der Vehikelgruppe. Auch auf die Lebensqualität der Betroffenen hatte Ruxolitinib einen positiven Effekt: Bereits 12 Stunden nach dem ersten Auftragen von 1,5 % RUX reduzierte sich der Juckreiz und die Patienten konnten besser schlafen. In den Wirkstoffgruppen wurden Nebenwirkungen – insbesondere ein Brennen beim Auftragen – seltener dokumentiert als in der Vehikelgruppe (0,6 bzw. 0,8% im Vergleich zu 4,4%). Im Studienzeitraum vereinzelnd aufgetretene schwere Nebenwirkungen konnten nicht mit der Anwendung von Ruxolitinib in Zusammenhang gebracht werden.
TRuE-AD1 und TRu-AD2 umfassten eine breite Patientenpopulation mit unterschiedlichem Krankheits¬schweregrad und Leidensdruck. In beiden Studien war Ruxolitinib signifikant besser wirksam als das wirkstofffreie Vehikel. Auffällig war der schnelle, klinisch relevante Rückgang des Juckreizes, vermutlich weil die Hemmung von JAK1 die Weiterleitung des Juckreizes in den sensorischen Nervenfasern verhindert. Bei Patienten, die Ruxolitinib erhielten, verbesserte sich der Schlaf, mit vermutlich positiven Auswirkungen auf die Leistungsfähigkeit, Lebensqualität und geistige Gesundheit. Da so gut wie keine Nebenwirkungen auftraten, bietet sich die Therapie bei schweren Verläufen als Alternative zur systemischen Therapie an. Als nächstes sollte die topische Anwendung von Ruxolitinib in klinischen Studien im Vergleich zu bewährten AD-Therapien getestet werden.
K. Papp et al. (2021). Efficacy and safety of ruxolitinib cream for the treatment of atopic dermatitis: results from 2 phase 3, randomized, double-blind studies. J. Am. Acad. Dermatol. 85(4): 863-872.